Sterowana regeneracja kości z użyciem allogenicznej płytki kortykalnej
Sterowana regeneracja kości z użyciem allogenicznej płytki kortykalnej
Opis przypadku – dr Carole Leconte (Paryż)
Regeneracja kości jest efektem złożonej techniki, ale też magii procesów tkankowych. Postęp, jaki dokonał się w ostatnich kilku latach, spowodował poddanie w wątpliwość wielu obowiązujących dotychczas dogmatów, ale pozostawmy na jakiś czas te śmiałe dokonania na należnym im piedestale, jako że są one kwintesencją wykorzystania wiedzy, zręczności chirurga stomatologicznego oraz potencjału gojenia danego pacjenta. W każdej sytuacji klinicznej możliwych jest zazwyczaj kilka sposobów postępowania terapeutycznego. Ich różnorodność pokazuje, że kilka różnych metod leczenia, często bardzo odmiennych, może przynieść oczekiwany skutek. Dlatego też nie należy wrzucać technik rozszczepania wyrostka, technik kanapkowych czy tunelowych do jednego worka technik biologicznych i przeciwstawiać im technikę sausage (kiełbaski).
Osobiście uważam, że przyszłość to umiejętność zrozumienia oraz nabierania wprawy i biegłości w różnorodnych technikach zabiegowych. W tej publikacji skupię się jednak na opisie decyzji i wyboru procedur chirurgicznych stosowanych w konkretnym przypadku klinicznym, które mogą być reprezentatywne dla podobnych przypadków i stanowią powtarzalną opcję terapeutyczną. pozwalającą na osiągnięcie wysoce satysfakcjonującego wyniku.
W naszym przekonaniu możliwości, jakie mamy obecnie do dyspozycji jedynie w części odzwierciedlają postęp w dziedzinie rekonstrukcji kości, natomiast to, czym dysponowaliśmy wcześniej, wydaje się być dziś odległą przeszłością i możemy tylko mieć nadzieję, że w przyszłości uzyskamy jeszcze bardziej przewidywalne i długoczasowo stabilne wyniki leczenia.
Jakie są możliwości zwiększenia pionowego wymiaru kości w odcinku bocznym żuchwy?
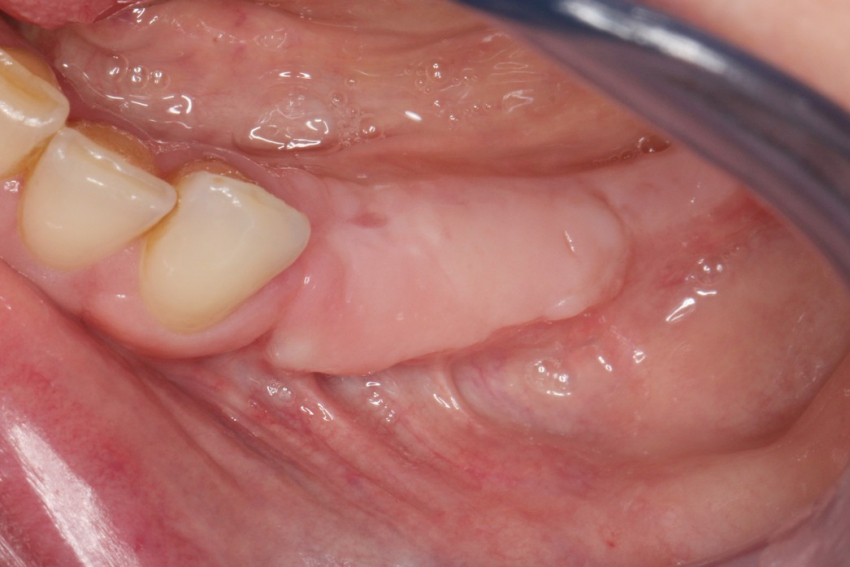
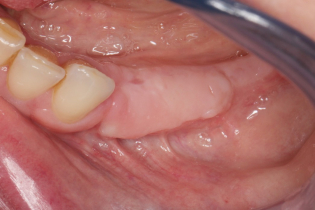
Przy podejmowaniu jakiejkolwiek decyzji musimy przeanalizować związane z nią potencjalne korzyści i ryzyka. Pacjentka (wiek 59 lat) zgłosiła się do naszego gabinetu z zawansowaną pionową utratą tkanki kostnej w żuchwie, spowodowaną przez wolno postępujące zapalenie przyzębia w trzecim kwadrancie uzębienia. Badanie CBCT (Cone Beam Computed Tomography – tomografia komputerowa wiązki stożkowej) wykazało, że możliwe jest w tym przypadku wprowadzenie krótkich implantów.
Naszą pierwszą myślą było przeprowadzenie prostego zabiegu o przewidywalnych rezultatach, aby uniknąć leczenia operacyjnego, które mogłoby być postrzegane jako działania nadmierne. Leczenie takie byłoby szybsze, obarczone mniejszym ryzykiem powikłań i tańsze. Jakość dostępnej kości była dobra, co sprzyjało możliwości przeprowadzenia leczenia minimalnie inwazyjnego.
Bardzo istotny był jednak zakres pionowej utraty kości: wynosił on około 7 mm. Stanęliśmy więc w obliczu niemal całkowitego braku grzbietu wyrostka zębodołowego. Wprowadzenie implantów na poziomie przyczepów mięśniowych, bez dziąsła przyczepionego, nie pozwoliłoby na zapewnienie prawidłowej higieny jamy ustnej. Ponadto wprowadzenie krótkich implantów w takim przypadku skutkowałoby powstaniem niekorzystnej proporcji między długością implantu i korony protetycznej. Zagadnienie to wzbudza często kontrowersje, niemniej jednak wydaje się być czynnikiem istotnym.
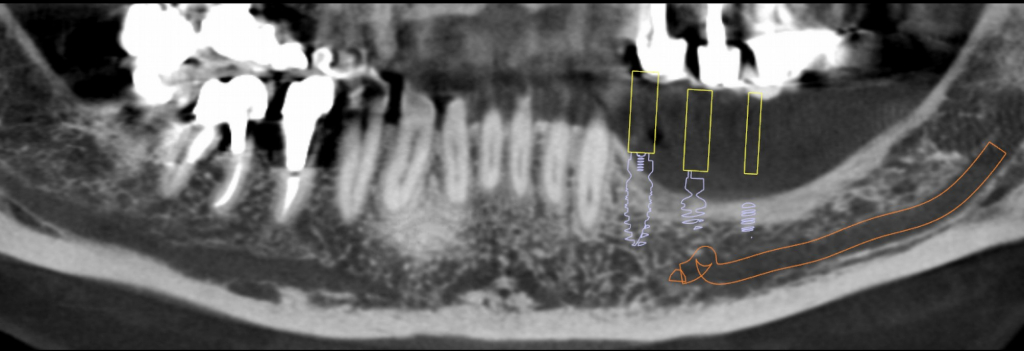
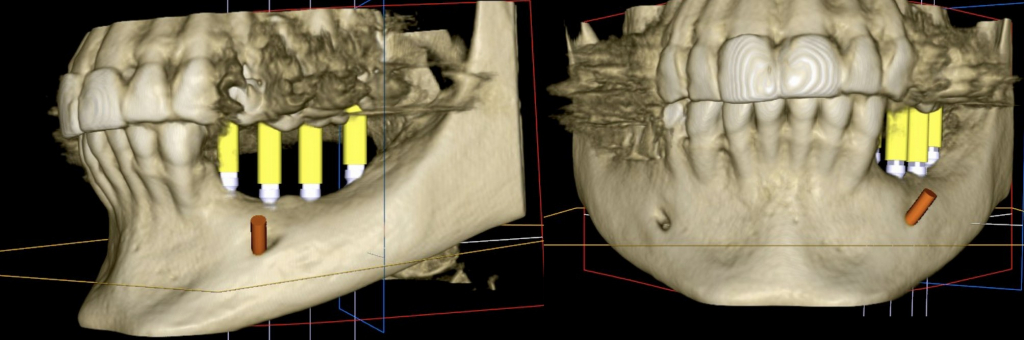
Równolegle do analizy aktualnej sytuacji klinicznej mającej na celu ocenę możliwych konsekwencji wyboru metody leczenia, próbowaliśmy określić możliwe czynniki ryzyka. Oczywiście najważniejsze były czynniki miejscowe wiążące się z takim zabiegiem: wprowadzenie implantu w sytuacji bardzo wąskiego wyrostka z zastosowaniem niepewnego biomateriału – dwufazowego cementu kostnego, brak obecności dziąsła skeratynizowanego.
Aby zredukować ryzyko wystąpienia periimplantitis, celowym wydawało się, aby przed wprowadzeniem implantów odtworzyć najpierw część kostną wyrostka, a następnie część dziąsłową. Im bardziej zaawansowana jest technika zabiegu, tym bardziej wzrasta prawdopodobieństwo wystąpienia powikłań, czasami trudnych do przewidzenia.
Ponadto, im poważniejsze zabiegi chirurgiczne przeprowadzamy u pacjentów z przebytymi w przeszłości zmianami w przyzębiu lub z przebytym periimplantitis, tym bardziej musimy starać się minimalizować ryzyko, rozdzielać kolejne etapy i stopniowo weryfikować, czy wstępny plan leczenia pozostaje w dalszym ciągu najkorzystniejszą opcją postępowania. Musimy wykonać sumienną pracę, a nie zrobić coś szybko i pobieżnie.
Wyjaśniamy zatem pacjentce znaczenie rekonstrukcji grzbietu wyrostka: odtworzenie korzystnych warunków anatomicznych, uzyskanie dużej objętości kości wokół implantów, oddalenie się od poziomu przyczepów mięśniowych sprzyjające w przyszłości łatwiejszemu utrzymaniu higieny, możliwość wykorzystania wolnego przeszczepu dziąsłowego (płata nabłonkowo-łącznotkankowego) pozwalającego na pogłębienie przedsionka oraz uzyskanie szczelnego połączenia z pojedynczymi koronami bez konieczności stosowania cementu.
Wyjaśniamy też, jakie ryzyka są związane z tym typem zabiegu: rozejście się brzegów rany pooperacyjnej, uszkodzenie nerwu bródkowego, infekcje/zakażenia wtórne, a także ryzyko wystąpienia resorpcji w dłuższej perspektywie czasowej.
Po wyjaśnieniu powyższych kwestii, początkowo rozczarowana pacjentka zaczęła stawać się naszym sojusznikiem. Przedstawiony plan leczenia stał się dla niej sensowny, gdy zrozumiała nasze wyjaśnienia. Położyliśmy nacisk na kwestie wpływu jej ogólnego stanu zdrowia/procesów biologicznych/potencjału gojenia organizmu na ostateczny wynik leczenia. Rzeczywiście zależy nam na tym, aby mieć pewność, że pacjenci w pełni zrozumieją, iż wyniki leczenia mogą być bardziej lub mniej satysfakcjonujące i stabilne w zależności od ich stylu życia, występujących u nich niedoborów itp. Pacjenci odgrywają bardzo istotną rolę w osiągnięciu sukcesu lub w niepowodzeniu leczenia.
Czy materiał augumentujący w formie rozdrobnionej (granulat) zapewnia większą stabilność?
Zagadnienie przewidywalności ma ogromne znaczenie, zwłaszcza gdy chodzi o augmentację pionową kości w bocznym odcinku żuchwy. Wiemy, że użycie rozdrobnionej kości w formie granulatu jest w aspekcie rewaskularyzacji i osteogenezy o wiele korzystniejsze, niż wykorzystanie bloków kostnych.
Wiemy, że nie wszystkie biomateriały zapewniają uzyskanie takich samych rezultatów. Pod względem stabilności kortykalno-gąbczaste materiały allogeniczne przypominają kość dwufazową, zapewniając optymalną równowagę między stabilnością (czasem osteogenezy) a resorpcją (umożliwiającą tworzenie się nowej kości autogennej). Biomateriały mają w swoim składzie również kolagen (chemotaksja, angiogeneza).
Musimy sobie wyobrazić, że tak, jak to jest w przypadku implantów, proces gojenia kości wokół biomateriałów to w pierwszej fazie również etap stabilizacji, a po uzyskaniu integracji następuje faza wtórna. Tak więc zabieg sterowanej regeneracji kości (GBR) można postrzegać jako proces 2-fazowy: stabilizacja początkowa związana z uzyskaniem objętości/gęstości/stabilności biomateriału, a potem stabilizacja wtórna związana z osteogenezą zachodzącą wokół cząstek biomateriału, a na końcu stabilizacja tkanki kostnej zależna bezpośrednio od biologii pacjenta.
Którą technikę wybrać? Jak ustabilizować objętość augmentacji pionowej kości w żuchwie?
Głównym problemem błon PTFE (politetrafluoroetylenowych) wzmacnianych tytanem było odcięcie obwodowego dopływu krwi wpływające na spowolnienie osteogenezy, co prowadziło do słabszego unaczynienia kości w jej peryferyjnych obszarach, gdzie będzie ona zatem prawdopodobnie mniej stabilna po usunięciu błony.
Technika biologiczna doktora Fouada Khoury’ego stanowi tutaj niewątpliwie trudny do pobicia punkt odniesienia. Jednakże jest ona związana z dość długim zabiegiem chirurgicznym, bardziej inwazyjnym i generalnie trudniejszym do wykonania.
Liczne analizy preparatów histologicznych pozyskanych w związku z wykonywanymi przez nas zabiegami GBR oraz moje osobiste, obecnie dziewięcioletnie doświadczenie obejmujące w praktyce ponad 1985 przeszczepów GBR i zabiegów sinus-liftu z wykorzystaniem kości z banku tkanek, upoważnia nas do potwierdzania wysokiej jakości dokonanych rekonstrukcji, jeśli warunki operacji były optymalne, a dobór pacjentów został dokonany prawidłowo.
Do chwili obecnej wykonaliśmy ponadto 45 rekonstrukcji metodą GBR/ACP (z wykorzystaniem allogenicznej płytki kortykalnej) wzorując się na technice doktora Fouada Khoury’ego oraz korzystając z pomocy i doświadczenia doktorów Enguerrana i P. Kellera.
Na dzień dzisiejszy postępujemy następująco: aby zwiększyć pionowy wymiar wyrostka w żuchwie, stosujemy płytkę allogenicznej kości kortykalnej w formie daszka, a pozostała część zabiegu może być porównana do tradycyjnej metody GBR z użyciem małych granulek kości kortykalno-gąbczastej (pozyskanej z banku tkanek BIOBank) i wolno resorbowalnej membrany kolagenowej (Créos-Nobel Biocare) stabilizowanej, jeśli jest to potrzebne, kilkoma pinami kostnymi (stabilizacja pinami jest regułą w przypadku zabiegu GBR z użyciem techniki sausage, natomiast w technikach z użyciem płytek stabilizacja nie zawsze jest konieczna, zwłaszcza w żuchwie).
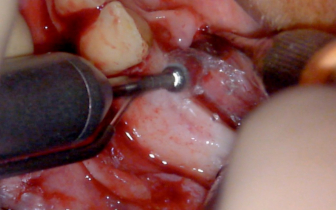
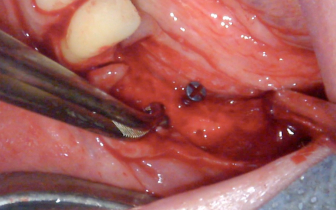
Przygotowanie pola zabiegowego. Cięcie na środku pozostałego dziąsła skeratynizowanego
Koniecznie jest wytworzenie płata tkankowego pełnej grubości odsłaniającego kość do wysokości górnej krawędzi bródki. Po podniesieniu płata można zebrać za pomocą skrobaczki wióry kości autogennej. Jest bardzo prawdopodobne, że pobudzi to osteogenezę i aktywuje biomateriał (dostarczając do jego obszaru białka autogenne). W tym konkretnym przypadku nie widzieliśmy takiej potrzeby.
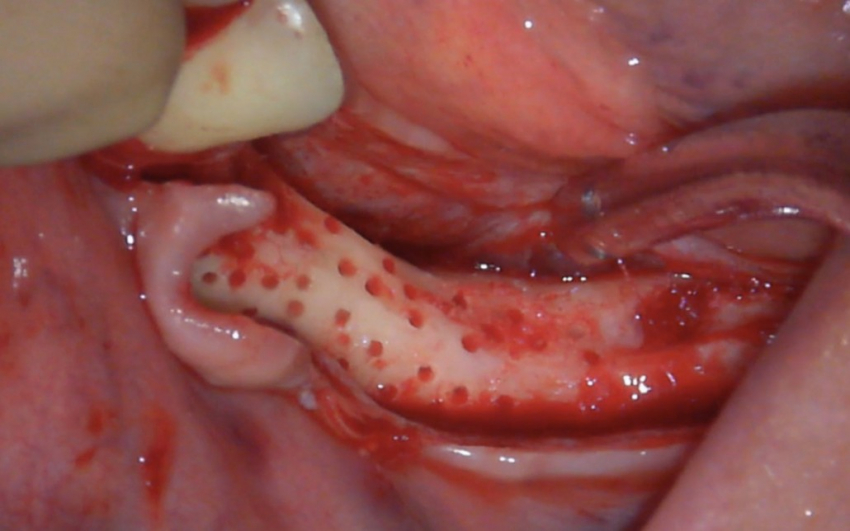
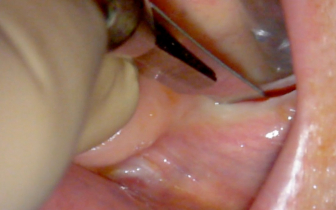
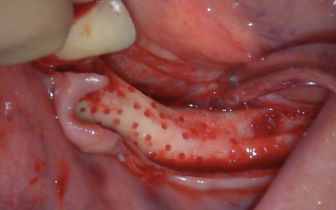
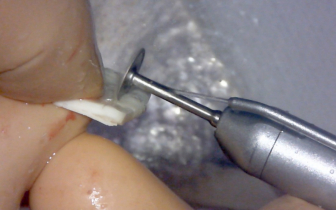
W bardzo interesującym badaniu z dziedziny histologii przeprowadzonym przez zespół doktora Dorigttiego De Avalia wykazane zostało, że korzystne jest wykonywanie mini-perforacji blaszki kortykalnej kości. Należy jednak uważać, aby nigdy nie używać wiertła o średnicy większej, niż średnica stosowanych później śrub do osteosyntezy czy też stępionych wierteł, mogących działać szkodliwie poprzez przegrzewanie kości w miejscu biorczym. Na koniec przeprowadza się plastykę allogennej płytki kortykalnej. Należy ją odpowiednio przyciąć i wygładzić krawędzie (stosując diamentowe wiertło lub krążek).
Jak ustabilizować płytkę?
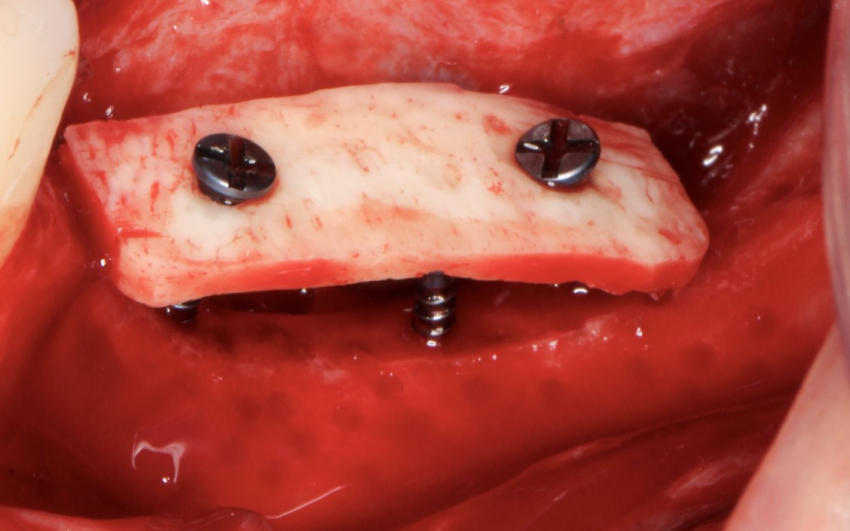
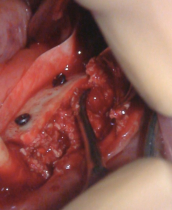
Stabilizacja pionowa płytki może, ale nie musi być problemem! Proponuję zacząć od wprowadzenia śruby podporowej wyznaczającej pozycję referencyjną dla pozycjonowania płytki. Powinna ona zostać wkręcona w kość w środku rekonstruowanego obszaru. Należy jednak zwrócić uwagę na to, aby nie wprowadzić jej w miejscu, w którym w przyszłości planujemy wprowadzenie implantów, gdyż śruba ta nie będzie usuwana. Najlepiej zastosować śrubę o średnicy 1,2 mm, aby nie zaburzała ona w przyszłości regeneracji biologicznej obszaru między implantami.
Tak naprawdę to wkręcenie śrub do osteosyntezy w grzbiet wyrostka pod różnymi kątami jest już wystarczające dla uzyskania dobrej stabilizacji pytki i utrzymania przeszczepu w pożądanej odległości od grzbietu wyrostka. Użycie śruby podporowej jest jedynie dodatkowym elementem, służącym ułatwieniu pozycjonowania płytki.
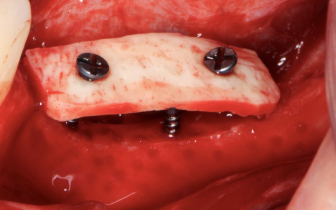
Następnie, po wykonaniu w płytce dwóch nieznacznie szerszych, nawierconych wstępnie otworów pilotujących, możemy ustabilizować ją dwoma śrubami do osteosyntezy o średnicy 1,5 mm (są wytrzymalsze, niż śruby o średnicy 1,2 mm) o długości ustalonej po zmierzeniu głębokości otworów sondą periodontologiczną. Dzięki śrubie podporowej i dwóm śrubom fiksacyjnym płytka powinna uzyskać idealną stabilność.
Tradycyjny zabieg GBR
Pozostała część zabiegu to zwykłe wypełnienie utworzonej przestrzeni. Pierwszą wolno resorbowalną błonę kolagenową (w tym przypadku była to błona Créos) umieszczamy od strony językowej.
Krew pozyskana podczas odwarstwiania płata na początku zabiegu zostaje zmieszana z biomateriałem (w tym przypadku były to małe granulki kości kortykalno-gąbczastej z banku tkanek BioBank). Oprócz tego, że krew pełni integralną rolę biologiczną (płynny narząd odpowiedzialny za proces gojenia), ułatwia ona również po zmieszaniu z biomateriałem jego wprowadzanie za pomocą szpatułki. Biomateriał zostaje następnie wprowadzony pod płytkę zarówno od strony językowej jak i przedsionkowej z jego lekką kondensacją. Zalecamy również pokrycie płytki cienką warstwą biomateriału.
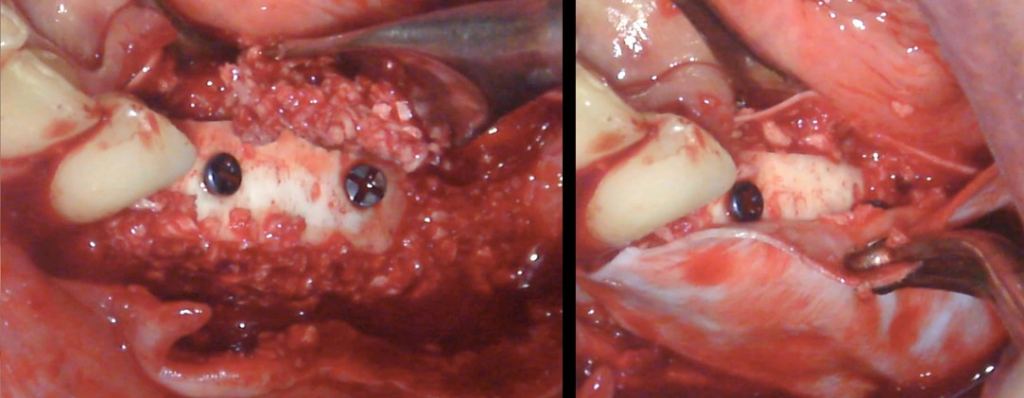
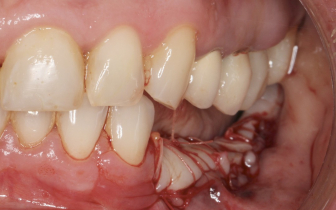
Drugą błoną kolagenową pokrywamy całość, wychodząc dość daleko poza obszar augmentacji. Zaszycie rany pozabiegowej jest jednym z najważniejszych etapów warunkujących powodzenie zabiegu, jest też jednym z najbardziej wrażliwych technicznie etapów postępowania. Wykonujemy dwa podcięcia okostnej – od strony językowej i przedsionkowej. Połączenie płatów bez napięcia musi być przeprowadzane z bezpiecznym zapasem, tak aby było możliwe położenie płatów naprzeciwko siebie bez ich cofania się. Szwy nie powinny nigdy być zakładane w sposób utrzymujący płaty brzeg do brzegu, ale w postaci wewnętrznych szwów materacowych powodujących wywinięcie krawędzi płatów. Poniżej obraz powłoki skórnej po 6 dniach od zabiegu. Zazwyczaj ból nie występuje lub występuje jedynie ból o niewielkim nasileniu.
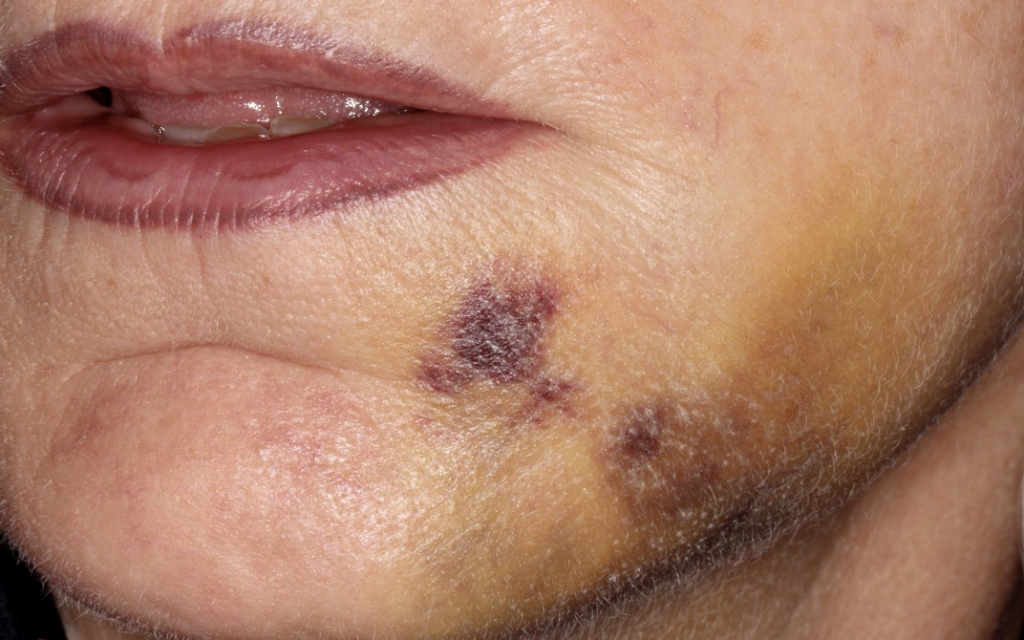
Gojenie kości, a potem działania kształtujące tkanki miękkie
Czas wstępnego gojenia obszaru przeszczepu kostnego (BGR) wynosi około 6 dni. Bazując na naszym doświadczeniu wiemy, że jest o wiele łatwiej wykonać przeszczep tkanki dziąsłowej na zrekonstruowanym grzbiecie wyrostka, niż na płaskim wyrostku (przed jego augmentacją).
Aby niepotrzebnie nie wydłużać czasu trwania leczenia, przygotowaliśmy następujący plan czasowy obejmujący wszystkie etapy postępowania:
– BGR > 4 miesięcy gojenia
– przeszczep nabłonkowo-łącznotkankowy z pogłębianiem przedsionka > 2 miesięcy gojenia
– implantacja.
Po 4 miesiącach gojenie kości jest już bardzo zaawansowane, co można zobaczyć na pooperacyjnym CBCT i na tym etapie nie zaburzą go już zabiegi na tkankach miękkich. Czas gojenia dziąsła może w ten sposób przebiegać równolegle z kończącym się procesem gojenia kości.
Analiza procesu gojenia kości
Kryteria oceny radiologicznej powodzenia zabiegu GBR to:
– wykształcenie się nowej blaszki kortykalnej
– zanik starej blaszki kortykalnej
– ubeleczkowanie w części środkowej
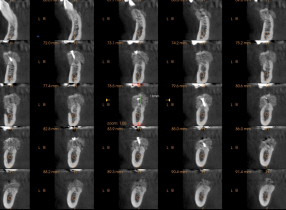
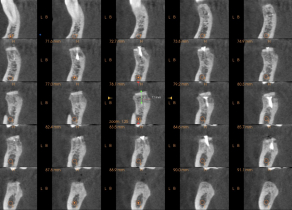
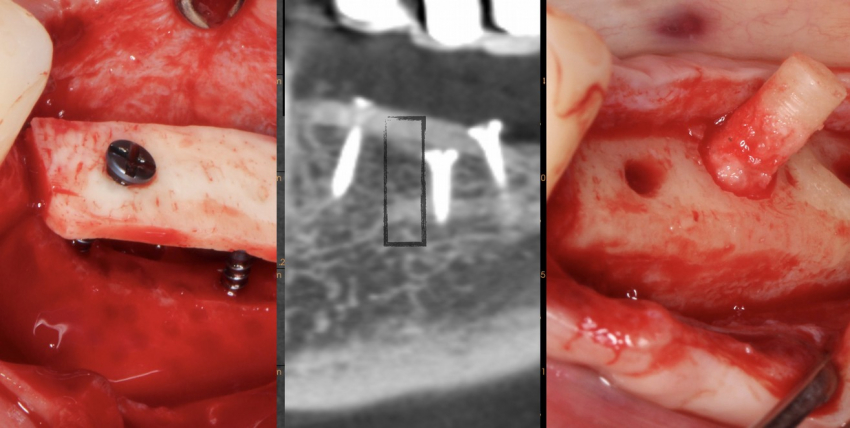
Obrazowanie 3D pozwala nam porównać sytuację przed, w dniu oraz po zabiegu. Można zauważyć, że w ciągu zaledwie 4 miesięcy formowanie blaszki kortykalnej na obwodzie jest już dalece zaawansowane (głównie po stronie przedsionkowej), podobnie jak widoczne jest ubeleczkowanie w części środkowej. W Państwa własnych porównaniach proponujemy oceniać tylko porównywalne okolice, jak na przykład obszar powyżej górnej granicy bródki. W tym przypadku przyrost wymiaru pionowego wynosi 7 mm. Widzimy też pewne zmiany. Osobiście nie postrzegam ich jako resorpcji ale jako przebudowę kości. Najważniejszą rzeczą jest nie tyle samo zachowanie objętości, co jakość biologiczna nowo uformowanej kości.
Przeszczep nabłonkowo-łącznotkankowy
Istotne jest, aby przed prowadzeniem skomplikowanych zabiegów implantologicznych opanować techniki chirurgii śluzówkowo-dziąsłowej. Wykonanie mobilizacji płata niezbędnego do zszycia brzegów tkanki pod koniec zabiegu GBR powoduje, że niemal zawsze niezbędne jest przeprowadzenie pogłębienia przedsionka, co wiąże się z czteromiesięcznym wgojeniem wolnego przeszczepu nabłonkowo-łącznotkankowego.
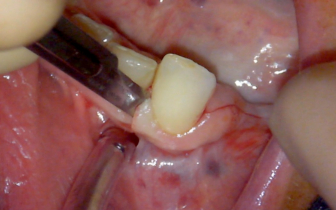
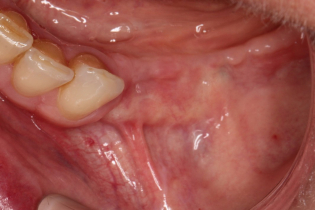
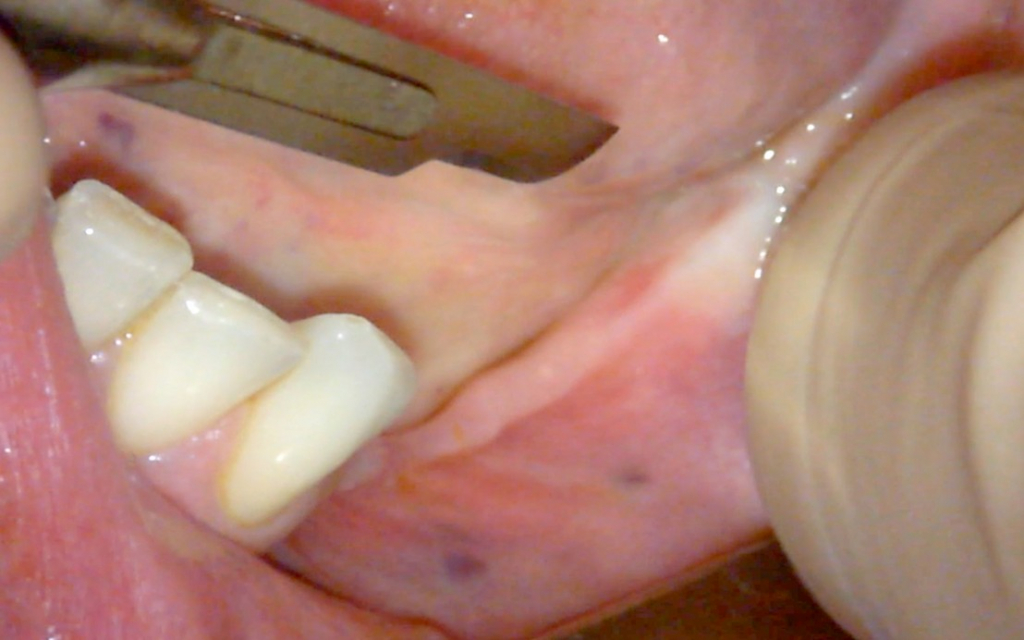
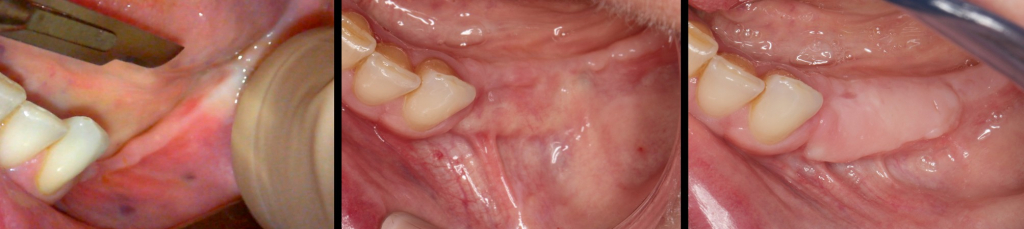
Pogłębianie przedsionka przeprowadzane jest od grzbietowej części pozostałego dziąsła skeratynizowanego, płatem częściowej grubości co najmniej 3 mm. Istotne jest uwzględnienie nowej głębokości przedsionka, który stanie się miejscem zakotwienia dla szwów stabilizujących w dnie przedsionka i implantów. Należy upewnić się, że została dokonana ocena, czy nie występują przeszkody natury anatomicznej. Widoczne poniżej szwy wykonano nicią 5/0 PGA Rapid.
Odsłonięcie i wprowadzenie implantów
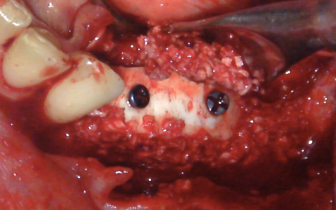
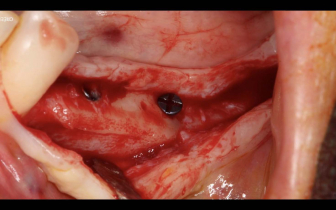
W tej technice odsłonięcie obszaru augmentacji nie pociąga za sobą konieczności odwarstwiania dużych płatów tkankowych, jako że trzeba usunąć jedynie dwie śruby z grzbietu wyrostka. Pozwala to uniknąć urazu tkanki kostnej związanego z koniecznością odwarstwiania tkanek przed usunięciem siatki tytanowej lub wzmocnionej tytanem błony PTFE. Zabieg implantacji jest raczej prosty i nie wymaga skomplikowanego odwarstwiania tkanek. Podczas zabiegu odsłaniania konieczna jest ocena jakości nowo uformowanej kości. W tym przypadku dokładnie widzimy rewaskularyzację wprowadzonego przeszczepu allogenicznego kości kortykalnej pozyskanej z banku tkanek. Od strony przedsionka, na poziomie wprowadzonego materiału w formie granulatu pokrytego błoną kolagenową, widzimy również piękną, nowo uformowaną kość kortykalną.
Dowodem jakości integracji biomateriału kostnego jest brak jakichkolwiek jego cząstek widocznych na powierzchni po 6 miesiącach. W przypadku obecności nieprzebudowanego, nieunaczynionego obszaru blaszki kortykalnej, wydaje się sensowne zniesienie jej wiertłem do miejsca wytworzenia obszaru żywej, nowo uformowanej kości.
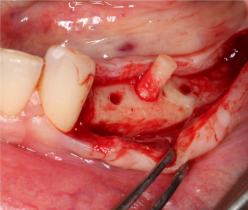
Po usunięciu śrub do osteosyntezy, ze środkowej części przeszczepu kostnego pobraliśmy (wiertłem o średnicy zewnętrznej 3 mm) próbkę do badania histologicznego. Gęstość, jakość i inne właściwości próbki były znakomite, porównywalne z kością klasy D1/D2.
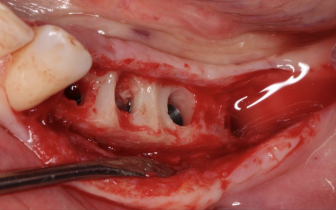
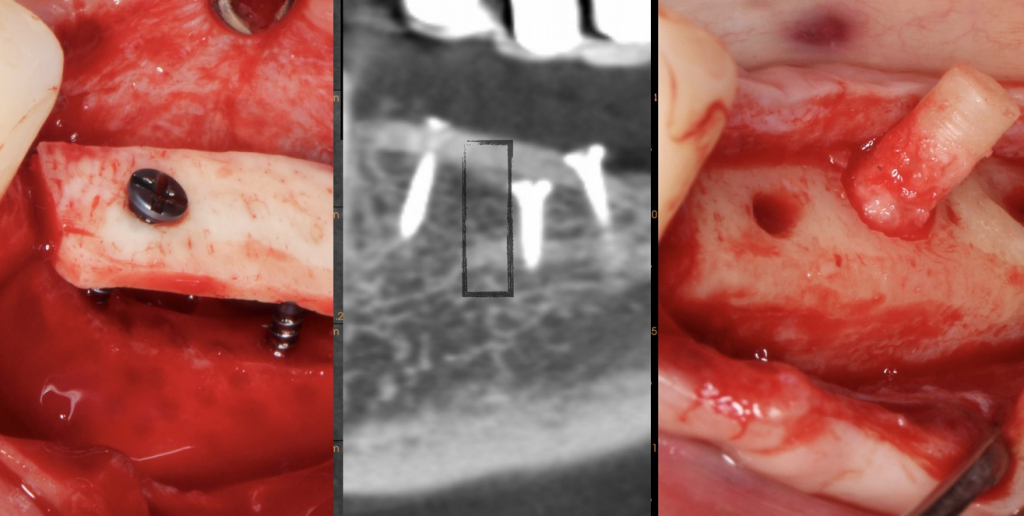
Na zdjęciu wykonanym podczas zabiegu wprowadzania implantów widoczna jest – pod dystalną krawędzią 35 mm otworu – główka pozostawionej śruby do osteosyntezy (śruba podporowa, znajdująca się na tym samym poziomie, co próbka do badania histologicznego). Brak zauważalnego klinicznie obszaru przejścia między płytką kostną, obszarem zrekonstruowanym za pomocą rozdrobnionej kości i poziomem kości sprzed zabiegu jest równie ważnym, mocnym kryterium oceny klinicznej. Pozostaje to w pełnej zgodności z niezwykle naturalnym obrazem radiologicznym.
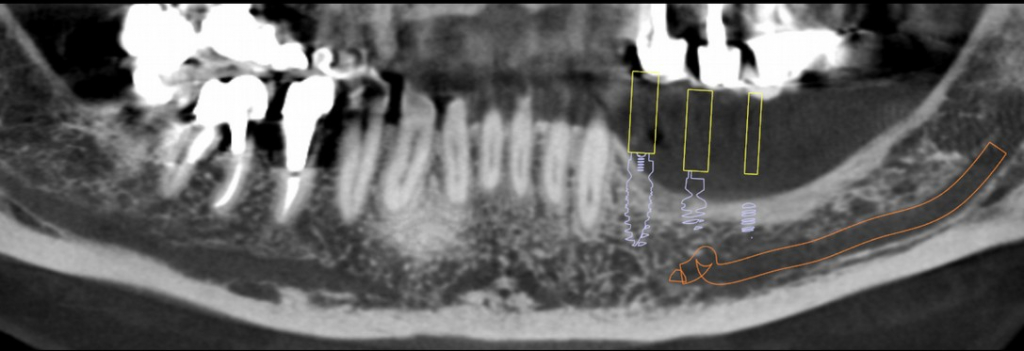
Jakość zrekonstruowanej kości pozwala na wprowadzenie czterech implantów (In-Kone Global D) poniżej poziomu blaszki kortykalnej (1,5 mm). Wprowadzamy je poniżej poziomu blaszki kostnej (subkrestalnie) jako dodatkowe zabezpieczenie. Implanty subkrestalne oraz typu tissue level to dwa rodzaje implantów, które wydają się zapewniać najlepszą stabilność tkanki kostnej na poziomie krawędzi implantu. Subkrestalne wprowadzenie implantów to dodatkowe zabezpieczenie, na wypadek wystąpienia wtórnych zmian w tym obszarze. Dlatego zalecamy takie rozwiązanie, aby zoptymalizować procesy biologiczne w obrębie tkanki kostnej na poziomie krawędzi implantu przy równoczesnej minimalizacji ryzyka.
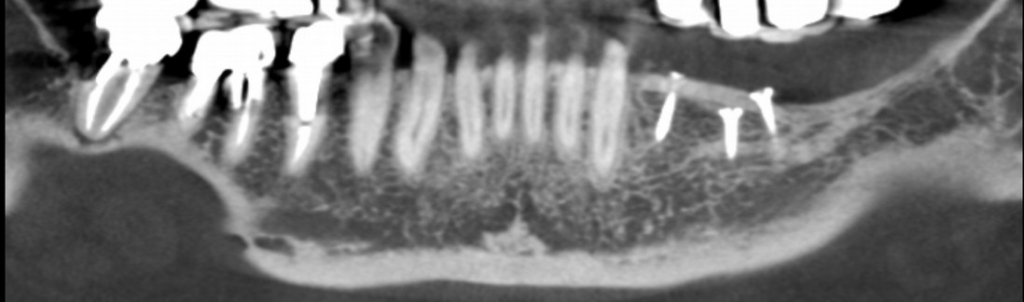
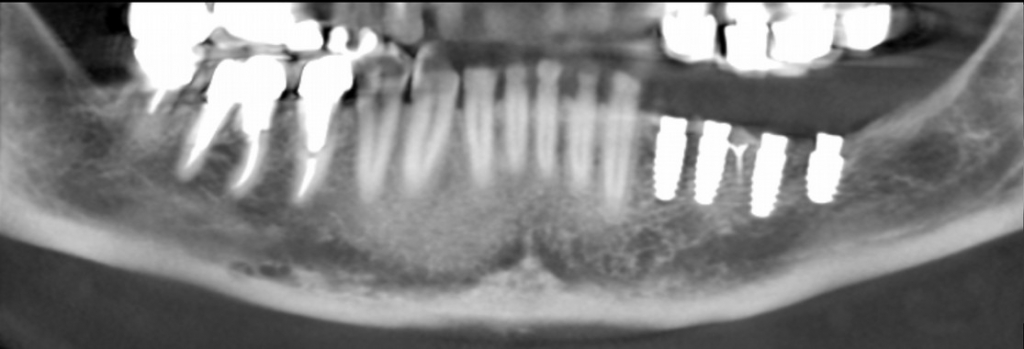
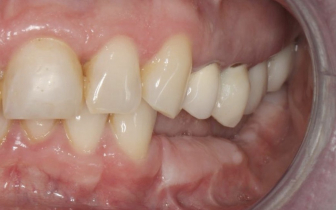
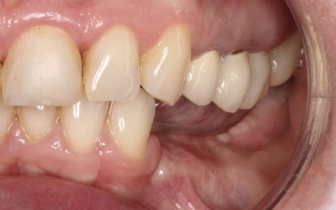
Możliwość wprowadzenia czterech implantów o standardowej długości pozwoli na zastosowanie czterech pojedynczych koron przykręcanych do implantów. Przykręcenie pojedynczych koron jest jedynym rozwiązaniem zapewniającym uzyskanie dobrej szczelności odbudowy na implancie (w tym przypadku zbieżność połączenia stożkowego wynosi 8°).
W celu zmniejszenia ryzyka nawrotu periimplantitis, które było traumatycznym przeżyciem dla pacjentki, wykonaliśmy następujące działania:
– dokładnie przyjrzeliśmy się jej stylowi życia w aspekcie zdrowotnym,
– wprowadziliśmy program poprawy i utrzymywania prawidłowej higieny jamy ustnej,
– zmieniliśmy kształt grzbietu wyrostka zębodołowego i wprowadziliśmy implanty w nowo uformowaną kość o odpowiedniej objętości i jakości, co pozwoliło na uzyskanie satysfakcjonującego poziomu kontaktu implantów z kością (BIC – Bone to Implant Contact),
– poprawiliśmy fenotyp dziąsła i odtworzyliśmy prawidłową głębokość przedsionka,
– wprowadziliśmy implanty pojedyncze, co pozwoliło na wykonanie pojedynczych koron przykręconych śrubami do tytanowych filarów tej samej marki co implanty, bez jakiegokolwiek negatywnego wpływu na kość oraz na zapewnienie szczelnego połączenia.
Analiza jakości procesu gojenia i porównanie stanu przed, w trakcie i po
Zalecamy wykonywanie zdjęć dokumentujących leczenie skomplikowanych przypadków, gdyż umożliwia to monitorowanie efektów wykonanych działań. W tym przypadku to cenne narzędzie umożliwiło ocenę zmiany sytuacji z bardzo negatywnej na korzystną.
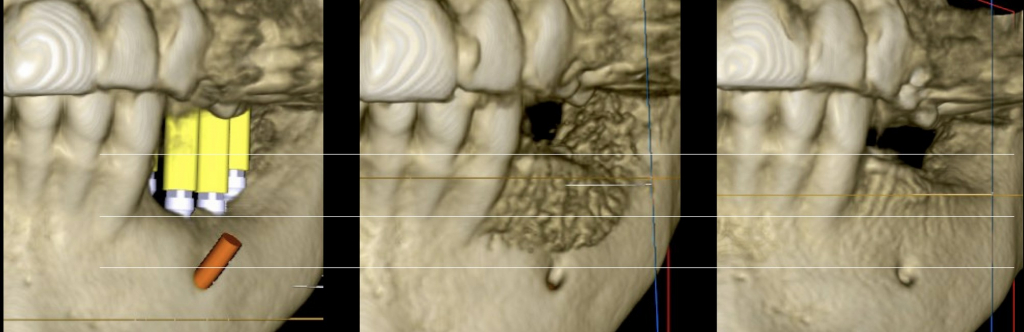
Ponadto minimalnym warunkiem umożliwiającym prawidłową analizę obrazu radiologicznego jest użycie urządzenia wysokiej jakości (w tym przypadku był to tomograf CBCT Carestream 9300) dającego możliwość wykonania:
– trójwymiarowych obrazów z wizualizacją nowej blaszki kortykalnej,
– trójwymiarowych obrazów pozwalających, po 4 czy 6 miesiącach, na radiologiczną ocenę powodzenia zabiegu GBR.
Staje się dla mnie coraz bardziej oczywiste, że musimy – i to bez dopuszczania jakichkolwiek kompromisów – oceniać efekty naszego leczenia, analizować tak obiektywnie, jak to tylko możliwe obraz przed i po zabiegu, ocenić sytuację w całej jej złożoności (cechy pacjenta, rodzaj defektu kostnego, wywiad medyczny) oraz badać zachowanie tkanek i stosowanych materiałów po zabiegu przeprowadzonym daną techniką.
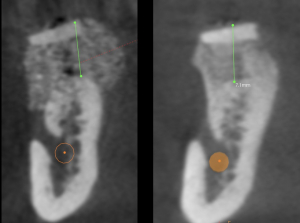 Nie należy wahać się przed pobraniem próbki kości do badania histologicznego. Jest to wciąż najlepsza metoda analizy jakościowej nowotworzonej kości. Jednak najważniejszymi, uniwersalnymi i miarodajnymi kryteriami są: dostrzegalna klinicznie i radiologicznie nowa blaszka kortykalna, proces beleczkowania oraz remodeling kostny. Musimy je oceniać w sposób usystematyzowany, aby móc „podpisać się” pod wykonanym z sukcesem zabiegiem chirurgicznym.
Nie należy wahać się przed pobraniem próbki kości do badania histologicznego. Jest to wciąż najlepsza metoda analizy jakościowej nowotworzonej kości. Jednak najważniejszymi, uniwersalnymi i miarodajnymi kryteriami są: dostrzegalna klinicznie i radiologicznie nowa blaszka kortykalna, proces beleczkowania oraz remodeling kostny. Musimy je oceniać w sposób usystematyzowany, aby móc „podpisać się” pod wykonanym z sukcesem zabiegiem chirurgicznym.
Im więcej czasu poświęcimy analizie zdjęć obrazujących sytuację przed zabiegiem i na etapie odsłonięcia obszaru augmentacji, im lepiej porównujemy obrazy radiologiczne na różnych etapach leczenia, tym większe korzyści płyną z naszej analizy i tym bardziej staje się ona obiektywna. Musimy być samokrytyczni.
Im bardziej zaawansowane są techniki zabiegowe, tym bardziej widoczny jest wpływ takich czynników jak umiejętności chirurgiczne operatora oraz potencjał biologiczny gojenia u pacjenta na efekt końcowy postępowania (oraz długoterminowe utrzymanie uzyskanego rezultatu).
Nie należy zapominać o fakcie, że biomateriały pomagają uniknąć pobierania materiału autogennego od pacjenta, ale nie zmieniają niczego, jeżeli chodzi o poziom technicznego skomplikowania rekonstrukcji i wykonywanie zabiegu podcinania tkanek miękkich, a także nie mają wpływu na zmienne zależne od pacjenta.
Nie możemy też zapominać o tym, że każdy z pacjentów ma indywidualny potencjał gojenia i jego jakość zależy od uwarunkowań genetycznych, higieny (ogólnej/jamy ustnej) i nierozsądne jest przeprowadzanie takich zabiegów na „niebezpiecznym gruncie”. Czy tego chcemy czy nie, gojenie zależy głównie od pacjenta.
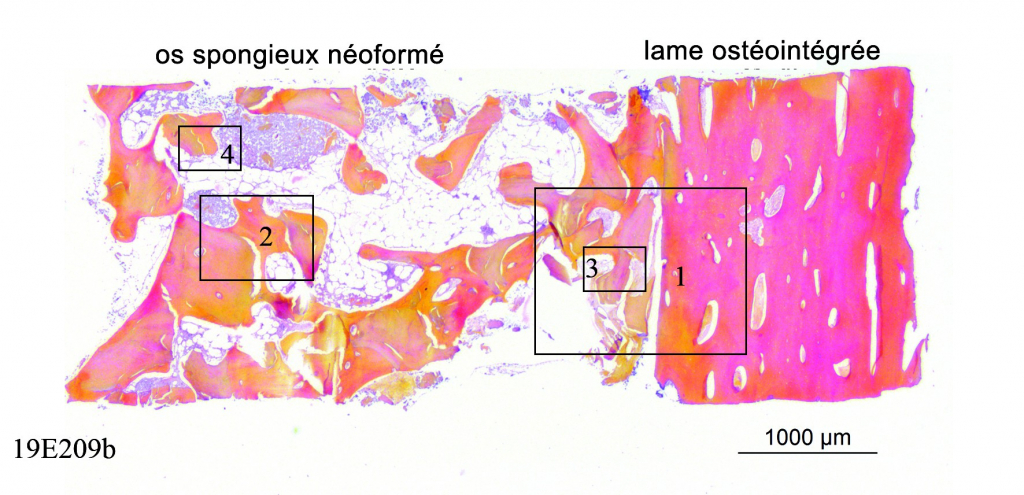
Badanie histologiczne jest najbardziej obiektywnym dowodem pozwalającym na dokonanie na poziomie komórkowym oceny rzeczywistej jakości nowo uformowanej kości i zachowania płytki z kości kortykalnej po gojeniu. W tym przypadku udział procentowy nowej kości w obszarze augmentacji jest bliski 50%. Tworzy się ona w kontakcie z materiałem augmentacyjnycm, co świadczy o jego jakości biologicznej/zdolności wiązania osteoblastów (badanie histologiczne preparatów barwionych hematoksyliną i eozyną w laboratorium Novotec w Bron).
Nasze spojrzenie na zabiegi w technice GBR wciąż ewoluuje. Jak wynika z naszych doświadczeń, połączenie allogennych płytek kości kortykalnej i granulatu kości kortykalno-gąbczastej pozwala skutecznie i z przewidywalnym rezultatem uzupełnić standardowy zabieg GBR. Daje to dodatkową możliwość leczenia w najbardziej skomplikowanych przypadkach, które, niestety, stają się zjawiskiem coraz bardziej powszechnym. Oczywiście mamy do dyspozycji również inne metody postępowania (na przykład osteodystrakcję czy bloki kości autogennej).
To nowe podejście uzupełnia jednak wachlarz naszych możliwości chirurgicznych i ogranicza ryzyko powikłań, pozwalając jednocześnie na osiągnięcie pożądanego celu odbudowy zarówno pod względem objętości jak i jakości kości. To właśnie przyświecało nam przy podejmowaniu decyzji o wyborze tej metody augmentacji.
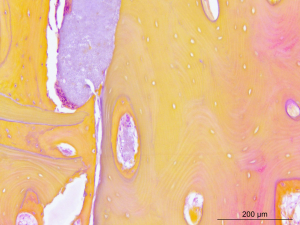
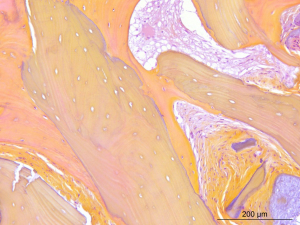
Nowa kość kortykalno-gąbczasta Płytka kostna po osteointegracji